復星醫藥近日宣布,將以約14.12億元人民幣收購綠谷醫藥51%股權,交易完成后綠谷醫藥將成為其控股子公司,核心產品甘露特鈉膠囊(商品名“九期一”)將納入復星醫藥創新藥管線。這一動作引發市場對阿爾茨海默病治療藥物研發進展的廣泛關注。
甘露特鈉膠囊作為全球自2002年美金剛獲批以來首個針對阿爾茨海默病的治療藥物,于2019年11月通過國家藥監局有條件批準上市,獲批適應癥為輕度至中度阿爾茨海默病患者認知功能改善。該藥品上市前已完成34家臨床研究中心參與的Ⅲ期確證性試驗,入組818例患者。根據有條件批準要求,上市后需繼續開展長期安全有效性研究及確證性臨床研究。
2024年該藥品原注冊批件五年有效期到期前,綠谷醫藥提交的補充申請未獲國家藥監局批準。監管部門明確指出,因上市后確證性臨床研究尚未完成,需繼續推進相關試驗。受此影響,自2024年11月起該藥品暫停商業化生產。上海證券交易所隨即向復星醫藥下發監管函,要求說明臨床試驗進展、核心技術問題及后續研發障礙等關鍵信息。
復星醫藥在27頁回復公告中披露,該藥品需完成正在進行的上市后確證性試驗并通過審評審批,同時獲得上海藥監局再注冊結論后方可恢復生產。公司透露已對試驗方案進行重大修訂:雙盲用藥期從36周延長至48周,樣本量由1312例增加至1950例,采用ADAS-Cog認知功能評估和ADCS-ADL日常生活能力評估作為雙主要終點。修訂方案已獲國家藥監局藥審中心認可,符合最新發布的阿爾茨海默病藥物臨床試驗技術指導原則。
臨床試驗推進情況顯示,該研究于2023年10月啟動首例受試者入組,截至2025年12月15日已完成580例入組。根據修訂后方案預估,2027年底完成全部受試者入組,2029年初完成研究并讀取數據,上半年提交臨床試驗總結報告。復星醫藥明確表示,目前未發現尚未解決的核心技術問題或實質性研發障礙。
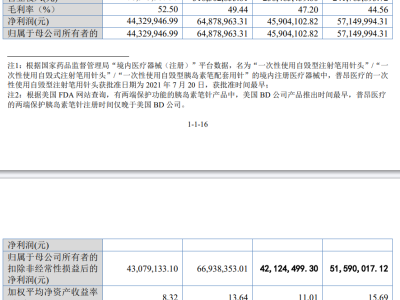
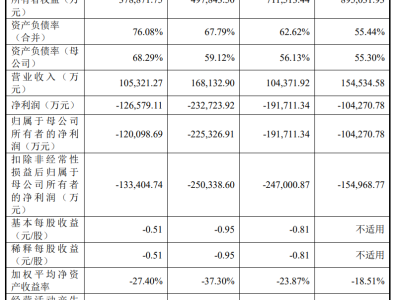
財務數據顯示,自2019年上市至收購前,甘露特鈉膠囊累計實現銷售額19.1954億元,銷售數量達677.11萬盒。2020-2024年完整銷售年度復合增長率約40%。研發支出方面,累計投入20.34億元,包括1.17億元專利費用、13.44億元國內研發投入(涵蓋上市前Ⅲ期試驗、真實世界研究及上市后試驗)以及5.73億元國際Ⅲ期試驗投入。
交易結構設計凸顯風險控制考量。復星醫藥采用“受讓存量股權+認購新增注冊資本”方式,總認購資金12.69億元分三期支付:首期6.35億元于交割日支付,剩余6.34億元根據后續研發進展在三年內支付。綠谷醫藥創始人控制的主體將質押10%股權作為風險擔保,形成動態出資機制以平衡臨床研發與投資風險。